ВЫТВОРЧАСЦЬ МАГНІЮ І ТЫТАНУ
§ 32. Вытворчасць магнію
Сыравінай для атрымання магнію служаць наступныя матэрыялы: карналіт MgCl₂ x KCl x 6H₂O (змяшчае 12 - 30% хлорыстага магнію), магнезіт MgCO₃ (звыш 45 % MgO), бішафіт MgCl₂ x 6Н₂О (звыш 46% MgCl₂). Магній атрымліваюць двума спосабамі: электролізам хларыдаў і тэрмічным аднаўленнем з руд.
Пры атрыманні магнію электралітычным спосабам з такой сыравіны, як магнезіт, спачатку атрымліваюць хларыд магнію. Для гэтага магнезіт падвяргаюць абпалу пры тэмпературы 850 - 900° З з мэтай выдалення СО₂ і атрыманні MgO. Затым хлараваннем у прысутнасці вугляроду атрымліваюць хларыд магнію: MgO + Cl₂ + С = MgCl₂ + СО. Атрыманы хларыд магнію падвяргаюць электролізу.
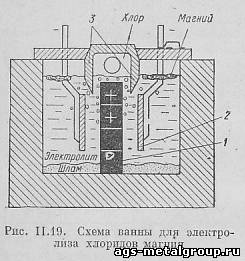
На мал. II.19 прыведзена прынцыповая схема адной секцыі ванны для электролізу хларыдаў магнію. Ванна прастакутнай формы мае вогнетрывалую футроўкі. Анодам служыць графітавая пласціна 1, катодамі - сталёвыя пласціны 2. Паміж анодам і катодам маецца перагародка 3 з шамотнай цэглы. У кожнай ванне збіраюць некалькі секцый, якія складаюцца з анодных блокаў і двух катодных пласцін. Сіла току ў ваннах дасягае 30 000 - 50 000, а пры напрузе ў 7 ст. Электралітам пры электролізе хлорыстага магнію служыць сплаў соляў: 8 - 16% MgCl₂, 25 - 35% CaCl₂, 25 - 35% NaCl і 18 - 25% KCl. Пры электролізе MgCl₂ раскладаецца. Хлор вылучаецца на анодзе, адкуль ён адсмоктваецца ў хлораправод і выкарыстоўваецца для хларавання вокісу магнію. На 1 т магнію атрымліваецца 2,9 т хлору. Магній выдзяляецца на катодзе. Бо магній лягчэй электраліта,
Для атрымання магнію ўжываюць і прасцейшыя тэрмічныя метады, якія складаюцца ў аднаўленні магнію з яго злучэнняў крэмніем, вугляродам і іншымі элементамі. Гэтыя спосабы дазваляюць выкарыстоўваць танныя віды сыравіны і паліва.
§ 33. Вытворчасць тытана
Прамысловае значэнне маюць тытаназмяшчальныя мінералы: ільменіт FeO X TiO₂ (змяшчае да 61% TiO₂), руціл TiO₂ (каля 10% вокіслаў жалеза, астатняе TiO₂), тытаніт, пероўскіт і інш.
Асаблівасці вытворчасці тытана абумоўлены яго высокай хімічнай актыўнасцю і вялікім сродством да кіслароду, азоту, вадароду і іншым элементам. Тытанавыя руды падвяргаюцца электрамагнітнаму, электрастатычнаму, флатацыйнаму, гравітацыйнаму і іншым відам узбагачэння, у выніку якіх атрымліваюцца канцэнтраты, якія змяшчаюць да 60% TiO₂. Рацыянальным спосабам перапрацоўкі жалезатытанавых канцэнтратаў з'яўляецца плаўленне ў электрычных печах. Аднаўленчай плаўкай атрымліваюць чыгун, легаваны тытанам (0,6 - 2,0% Ti), і дзындры, утрымоўвальныя каля 80% TiO₂ і 1,5 - 3,0% FeO, выкарыстоўваныя ў якасці сыравіны для атрымання тытана.
Атрыманне металічнага тытана з тытанавых канцэнтратаў або дзындраў зводзіцца да атрымання:
- тэтрахларыду тытану TiCl₄ уяўляе сабой вадкасць, кіпячую пры 136° З;
- тытанавай губкі аднаўленнем тэтрахларыду тытана;
- зліткаў кампактнага тытана з тытанавай губкі.
1. Атрыманне тэтрахларыду тытану з рутіла TiO₂ робіцца аднаўленнем вугляродам і хлараваннем пры 800° С па рэакцыі: TiO₂ + 2Cl₂ + 2С = TiCl₄ + 2СО.
2. Атрыманне тытанавай губкі робіцца аднаўленнем тэтрахларыду тытану магніем па рэакцыі: TiCl₄ + 2Mg = Ti + 2MgCl₂.
Працэс вядзецца ў сталёвых рэактарах пры тэмпературы 950 - 1000 ° С у атмасферы аргону або іншых інэртных газаў.
3. Атрыманне кампактнага пластычнага тытана з губкі часцей за ўсё ажыццяўляецца плаўленнем у электрычных дугавых або высокачашчынных печах. Схема дугавой печы з выдаткоўваным электродам прыведзена на мал. II.7. Плаўка вядзецца ў вакууме ці ў асяроддзі інэртных газаў. Пасля плаўлення атрымліваюць тытан, які змяшчае каля 0,2% прымешак, які адрозніваецца высокай пластычнасцю, добра які паддаецца пракатцы, каванню і штампоўцы.
Найболей чысты прамысловы тытан, утрымоўвальны меней 0,1% прымешак, атрымліваюць ёдыдным спосабам - раскладаннем ёдыдаў тытана на паверхні вальфрамавай ніткі, нагрэтай да 1300 - 1500° З у вакууме.
Асоба чысты тытан можа быць атрыманы з тэхнічнага тытана метадам зоннай плаўкі. Метад заснаваны на з'яве большай растваральнасці прымешак у вадкім метале ў параўнанні з растваральнасцю ў цвёрдым метале.
| 